如果以上都正常,還要確定下實驗過程中的操作細節。
比如在做標準曲線的時候是否是梯度稀釋的標準品,如果不是梯度稀釋標準品,可能會引起標準曲線擴增效率或者R2值異常;
從冰箱冷凍中取出的試劑是否有混勻,如果試劑融化后沒有混勻,這時候取出的試劑不是均一的,會影響后面的擴增;
定量PCR預混液跟核酸模板加好后是否混勻,如果沒有混勻,特別是樣本體積比較大的時候(超過PCR體系的20%),更容易發生optical mixing現象。
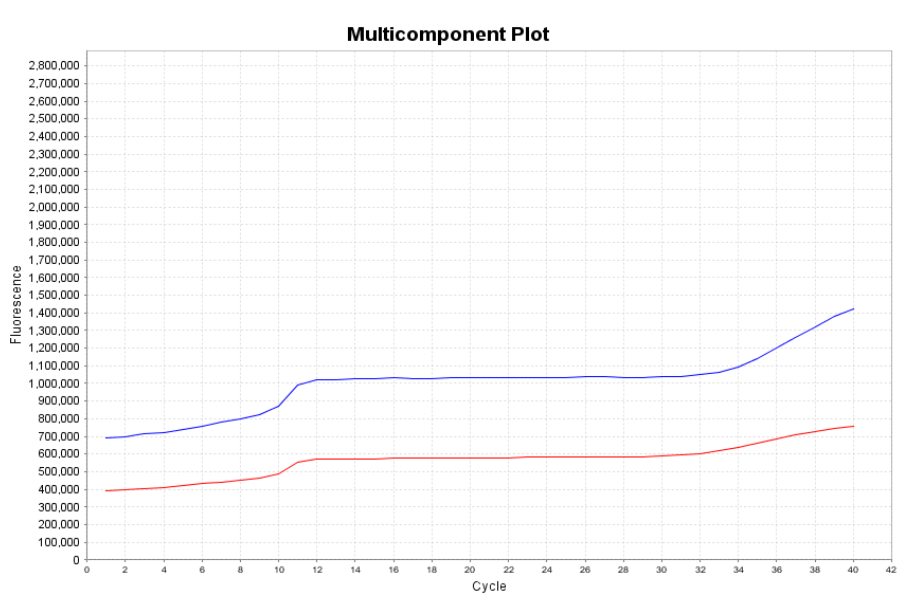
因為樣本是水相會在上層,試劑(含有甘油成分)會在下層,在前期的PCR過程中不足以混勻完全,這樣會形成折射,熒光較強,而一般加熱幾個循環后樣本跟預混液會混勻,熒光就變穩定了(圖十)。

圖十:樣本跟預混液未混勻現象
還有上機的反應體系里盡量不要有大的氣泡,有氣泡的話,中間容易形成折射,干擾熒光的采集(圖十一)。所以實時熒光定量PCR實驗的細節還是要特別注意的。
圖十一:反應體系中有氣泡

解決方案:將樣本稀釋后進行擴增(抑制物的影響可通過稀釋樣本消除)

手動設置基線。將Baseline End設置為“擴增信號出現的前一個循環”即,圖片展原始為26,將其設置為20,點擊OK即可恢復正常曲線。
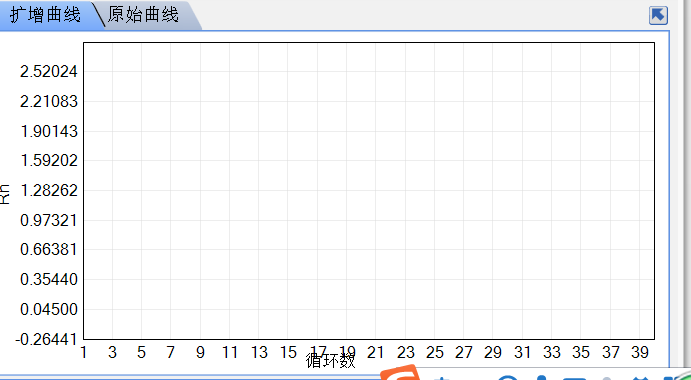
(1)PCR參數設置錯誤:在設計循環參數時沒有設置熒光信號采集;(2)模板降解: 避免樣品制備中雜質的引入及反復凍融的情況;(3)引物或者探針降解:可通過PAGE電泳檢測其完整性;
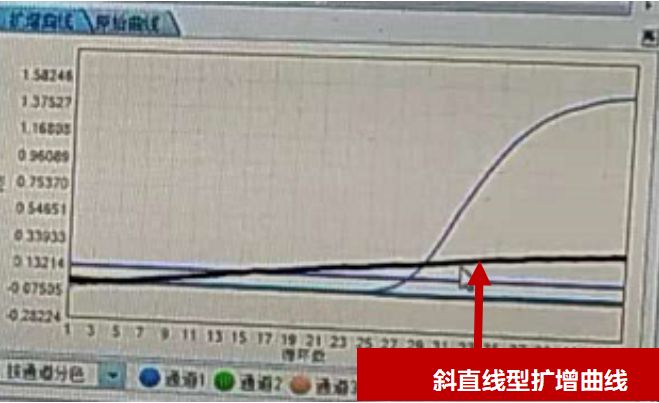
PCR實驗首次檢測呈斜直線型擴增曲線,再次復檢后結果基本均為正常陰性。- 分液不準確,檢查檢測后的反應管可發現管內的PCR反應液量明顯少于正常管;
- 反應管氣密性差,反應過程中溶液蒸發引起探針濃度增加,導至曲線呈斜直線狀。
- 分液均勻,上機前檢查八連管液面是否在同一水平線上;
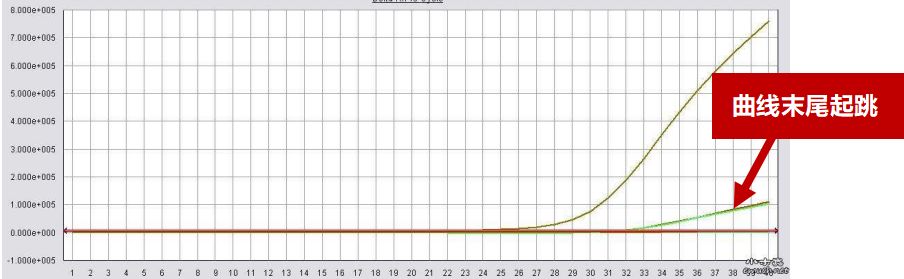
PCR實驗結果中有曲線出現末尾起跳但是沒有完整擴增的現象。
(3)正常樣本也可存在曲線末尾起跳,表示樣本濃度低或者加樣量不準確。- 排除污染原因后復檢樣本,如果復檢后曲線為陰性直線則說明之前的末尾起跳為非特異性擴增,如果復檢后曲線仍與之前一致則說明末尾起跳表示該樣本中待檢病毒核酸的濃度偏低。
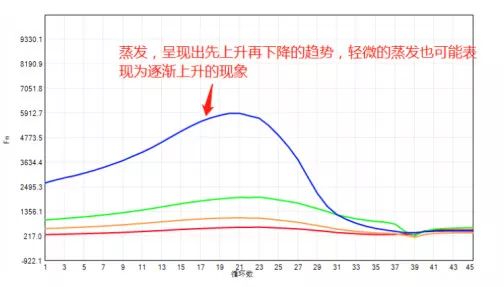
嚴重的蒸發會呈現先上升后下降的曲線,輕微的蒸發會是一種緩慢的上升,這兩類異常的曲線可以看一下檢測后的反應管液面是否有下降的現象來證明。
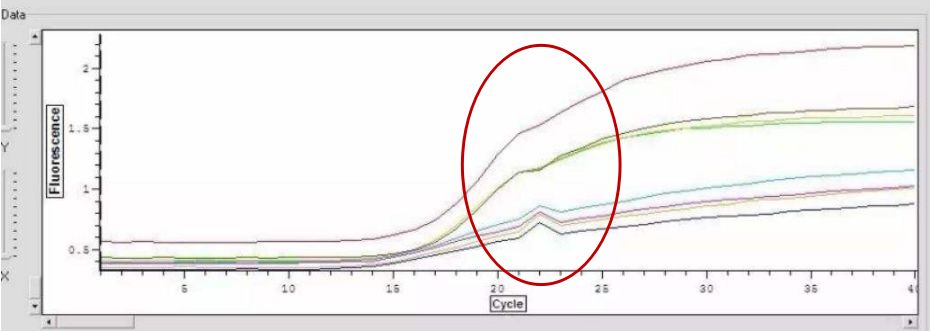
(1)儀器不穩定導至的擴增曲線異常(也可能突然停電或者電壓不穩);(2)如果尖峰向下,可能是鹵素燈老化所致發射光源不穩定(指鹵鎢燈光源的激發器)(3)如果是單一的孔位出現尖峰,除了考慮儀器或者孔位問題外,還要考慮反應體系是否有氣泡所致。qPCR實驗室面臨的最大問題就是核酸氣溶膠污染的問題,每個實驗室都要特別注意。