
美國生物技術巨頭安進(Amgen)近日公布了BiTE免疫療法Blincyto(blinatumomab)一項III期臨床研究(20120215,NCT02393859)的預先指定中期分析結果,顯示該研究的主要終點無事件生存期(EFS)已經達到。
該研究是一項開放標簽、隨機、對照、全球性多中心研究,評估了Blincyto與常規鞏固化療治療高危B細胞急性淋巴細胞白血病(ALL)患者首次復發時的療效、安全性和耐受性。由于在Blincyto治療組中觀察到的令人鼓舞的療效,根據獨立數據監測委員會(DMC)的建議,該研究的患者入組已提前終止。后續將繼續按臨床方案繼續推進。
此外,評估Blincyto用于兒童B細胞ALL患者首次復發時治療的一項隨機III期研究(COG AALL1331,NCT02101853),根據兒童腫瘤組(COG)DMC的建議,已關閉高風險組和中等風險組的患者入組。DMC的關閉決定基于Blincyto與化療相比在無病生存期(DFS)方面改善的強勁趨勢、總生存期(OS)的提高、顯著降低的毒性、更好的微小殘留病(MRD)清除。COG DMC建議AALL1331研究的低風險組繼續入組和隨機化患者,直至達到入組目標。AALL1331研究由美國國立衛生研究院(NIH)下屬的國家癌癥研究所(NCI)癌癥治療評估項目贊助,并由NCI資助的COG進行。安進根據NCI與安進的合作研究協議,為AALL1331研究提供Blincyto。
安進研發執行副總裁David M. Reese表示:“綜合考慮,這些研究的結果是顯著的。急性淋巴細胞白血病復發的兒童和青少年面臨著不良的預后,仍然需要額外的治療選擇,特別是那些被確定為高危的患者。這些數據有可能改變臨床實踐,并可能提供一種比化療更好的預防復發的治療方法。我們期待著與監管部門討論這些數據。”
在上述2項III期研究(20120215和COG AALL1331)中觀察到的Blincyto不良事件與Blincyto已知的安全概況一致。這些中期數據將在未來召開的醫學會議上公布。
Blincyto是全球獲批的首個也是唯一一個CD19-CD3雙特異性T細胞銜接(BiTE)免疫療法,同是安進BiTE技術平臺誕生的首個雙特異性抗體產品,能夠通過將腫瘤細胞上的CD19蛋白呈遞給T細胞特異表達的CD3蛋白,進而激活免疫系統識別并殺滅腫瘤細胞。
BiTE抗體技術代表了一種創新的免疫治療方法,能夠在很低濃度下起作用。安進于2012年耗資12億美元收購Micromet公司后獲得了BiTE技術。目前,安進正在廣泛的難治性腫瘤類型中,探索BiTE創新療法的潛力。
此前,美國FDA和歐盟EMA均已授予Blincyto治療多種類型血液癌癥的孤兒藥地位及突破性藥物資格和優先審查,包括急性淋巴細胞白血病(ALL)、慢性淋巴細胞白血病(CLL)、毛細胞白血病(HCL)、幼淋巴細胞白血病(PLL)和惰性B細胞淋巴瘤、套細胞白血病(MCL)等。
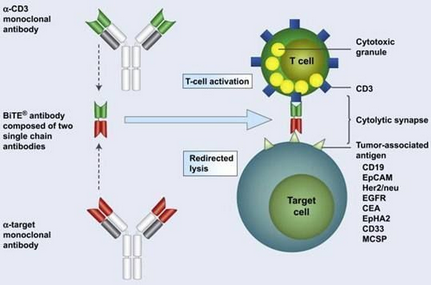
BiTE免疫療法作用機制
在美國,Blincyto已被批準用于治療:(1)復發性或難治性B細胞前體ALL成人和兒童患者;(2)在首次或第二次完全緩解時微小殘留病(MRD)≥0.1%的B細胞前體ALL成人和兒童患者。
在歐盟,Blincyto已被批準用于治療:(1)費城染色體陰性、CD19陽性、復發性或難治性急性淋巴細胞白血病(ALL)成人患者;(2)在首次或第二次完全緩解時微小殘留病(MRD)≥0.1%的費城染色體陰性、CD19陽性B細胞前體ALL成人患者;(3)在先前接受過至少2種療法后復發或難治、或在先前接受異基因造血干細胞移植后復發的費城染色體陰性、CD19陽性B細胞前體兒童患者(≥1歲)。
在ALL患者中,病情完全緩解后檢測殘留癌細胞(即MRD)是評估病情復發的最強預后因素。值得一提,在美國和歐盟,Blincyto是首個獲得監管批準根除MRD的療法。
去年12月12日,安進以278億美元收購Horizon的交易成為2022年最大一筆收購案。在經歷FTC的阻撓波折后,該筆重磅交易在本月6日正式敲定,收購總價278億美元。而近日,大約有350名Hori......
安進宣布olpasiran在針對脂蛋白(a)增高的II期OCEAN(a)-DOSE研究中獲得積極的關鍵結果。脂蛋白(a)由基因調控表達,在肝臟中產生,據報道是心血管疾病的獨立風險因素。病理生理學、流行......
2月7日,安進公布全年業績,全年總收入259.79億美元,美國全年產品銷售額下降4%,美國以外地區的全年產品銷售額增長12%,其中亞太地區增長36%。安進全年研發費用48.19億美元(+15%),占總......
最近,復旦大學附屬腫瘤醫院吳小華教授團隊在2020年歐洲腫瘤內科學會大會上(在線),分享了一項關于復發性卵巢癌PARP抑制劑治療的“中國方案”。該方案證實,接受PARP抑制劑藥物尼拉帕利維持治療的復發......
2020年8月27-29日,歐洲肝病學會(EASL)年會暨數字化國際肝臟大會(DILC)以線上會議形式隆重召開,這是EASL首次以“數字化會議”模式召開的年度盛會,吸引來自世界各地的科學和醫學專家了解......
3月9日,安進提交的AMG510臨床申請獲得CDE受理。AMG510是首個靶向KRASG12C的口服選擇性可逆抑制劑。 安進在ESMO2019大會上公布的AMG510治療實體瘤的I期臨床結果......
2月12日,君實登記啟動了其自主研發的人源化抗PD-L1單克隆抗體JS003的一項國內I期臨床研究,用來評估JS003在經治的晚期或復發性實體瘤受試者中的安全性、耐受性和劑量限制性毒性(DLT)。計劃......
今日,KiniksaPharmaceuticals公司宣布,美國FDA授予其在研IL-1信號通路抑制劑rilonacept突破性療法認定,用于治療復發性心包炎(RP)。Rilonacept將RP患者的......
急性淋巴細胞白血病(ALL)是兒童中最常見的癌癥。此外,對于患有21三體綜合征(唐氏綜合癥)的兒童來講,他們患ALL的幾率比沒有唐氏綜合癥的兒童高10到20倍。對此,來自貝勒醫學院的KarenR.Ra......
美國生物技術巨頭安進(Amgen)近日公布了BiTE免疫療法Blincyto(blinatumomab)一項III期臨床研究(20120215,NCT02393859)的預先指定中期分析結果,顯示該研......